近日,国际纳米生物交叉领域期刊《ACS Applied Materials & Interfaces》(JCR Q1分区,2025影响因子8.2)报道了我校“微纳生物技术”创新团队的研究成果“Biomineralization-Driven Interfacial Complexation at the Liquid Interface for Probiotic Delivery and Reactive Oxygen Species Scavenging” (DOI: org/10.1021/acsami.5c20280,译名:生物矿化驱动的界面自组装策略用于益生菌递送和活性氧清除)。论文第一作者为微密圈
2022级硕士研究生谢雯同学,通讯作者为苑昊副教授和孟涛教授,微密圈
为论文的唯一署名单位和通讯作者单位。

在液体界面集成功能性生物分子和纳米材料,是推动3D生物打印、生物催化和功能界面工程发展的基本策略,通过同步纳米材料的可调物理性质和生物分子的专用生物活性。然而,传统策略依赖特定的表面修饰剂,这往往会破坏生物分子和纳米材料的功能和活性,同时阻碍界面与周围环境的相互作用。本文介绍了一种简便且无修饰剂的方法,利用生物分子矿化(保持原生构象/功能)和具有相反物理化学性质的界面复合物(促进界面整合且无需修饰剂)构建生物分子-纳米颗粒集成功能界面。该方法满足了无修饰剂工程的关键需求,确保生物分子活性和纳米颗粒功能完整,并实现界面与周围环境的相互作用。为证明其实用性,我们将该策略应用于益生菌递送:界面共锚定生物分子(天然酶)和纳米颗粒(纳米酶),协同提升益生菌存活率,并实现了活性氧清除。这项工作为生物治疗建立了一个可扩展的平台,在这里界面生物分子和纳米颗粒的完整功能得以保留。除了治疗领域,这一策略还可扩展到需要高特异性、稳定性和可扩展性的协同生物分子-纳米颗粒相互作用的应用场景,如先进生物感测、高效生物能转换、定向环境修复和智能生物杂交材料。
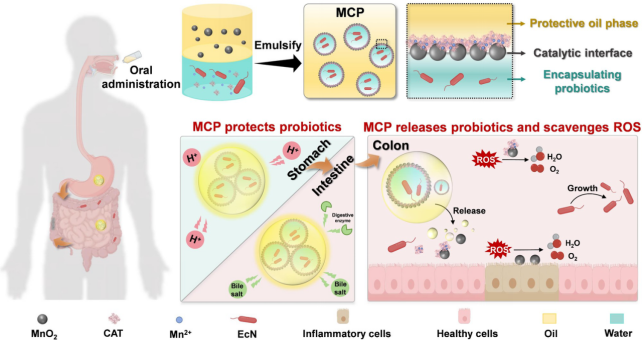
总结展望:本研究开发了一种无需表面修饰剂的生物分子(天然酶)-纳米材料(纳米酶)界面整合新策略。该策略利用矿化生物分子与纳米材料的理化性质互补,共锚定于液-液界面稳定Pickering乳液,同时保持了生物分子活性和纳米材料功能,成功解决了界面工程领域的长期难题。并将其应用于益生菌递送领域,可有效提升益生菌在胃肠道递送和活性氧攻击下的存活率。此外,该策略还可拓展至先进生物传感、生物能源转化、人工细胞膜构建等领域,为生物治疗制剂、生物杂化材料研发开辟了新途径。
该研究得到国家自然科学基金项目(22378336, 22204130, 21776230),四川省科技计划项目(2021YFN0129, 2022NSFSC1211)以及中央高校基础研究基金(2682024ZTPY001, 2682023ZTPY048)资助。感谢微密圈
分析测试中心的大力支持。
论文链接://doi.org/10.1021/acsami.5c20280
课题组主页://faculty.wei01.net/mengtao/zh_CN/index.htm
